Thể loại: Thợ điện Novice, Thợ điện công nghiệp
Số lượt xem: 37528
Bình luận về bài viết: 0
Ứng dụng thực tế của điện phân
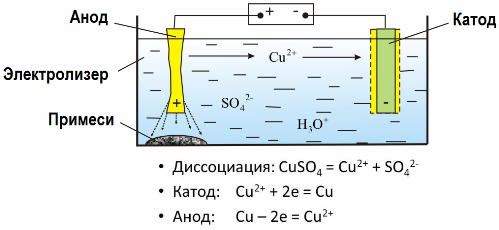
Khi một dòng điện đi qua dung dịch hoặc tan chảy chất điện phân, các điện cực hòa tan hoặc các chất khác là sản phẩm của các phản ứng thứ cấp trên các điện cực được giải phóng trên các điện cực. Quá trình hóa lý này được gọi là điện phân.
Bản chất của điện phân
Trong điện trường được tạo ra bởi các điện cực, các ion trong chất lỏng dẫn điện chuyển động theo thứ tự. Điện cực âm là cực âm, cực dương là cực dương.
Các ion âm được gọi là anion (ion của nhóm hydroxyl và dư lượng axit) chạy đến cực dương, và các ion dương gọi là cation (hydro, kim loại, ion amoni, v.v.) chạy về cực âm
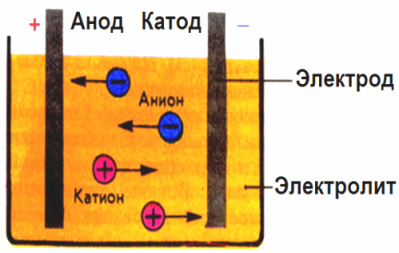
Một quá trình oxy hóa - khử xảy ra ở các điện cực: sự khử điện hóa của các hạt (nguyên tử, phân tử, cation) xảy ra ở cực âm, và quá trình oxy hóa điện hóa của các hạt (nguyên tử, phân tử, anion) xảy ra ở cực dương. Phản ứng phân ly trong chất điện phân là phản ứng chính và phản ứng xảy ra trực tiếp tại các điện cực được gọi là phản ứng phụ.
Định luật điện phân Faraday
Việc tách các phản ứng điện phân thành sơ cấp và thứ cấp đã giúp Michael Faraday thiết lập các định luật điện phân:
-
Định luật đầu tiên của điện phân Faraday: khối lượng của chất lắng đọng trên điện cực trong quá trình điện phân tỷ lệ thuận với lượng điện được truyền tới điện cực này. Theo lượng điện có nghĩa là một điện tích, được đo, như một quy luật, trong mặt dây chuyền.
-
Định luật thứ hai của điện phân Faraday: đối với một lượng điện nhất định (điện tích), khối lượng của một nguyên tố hóa học lắng đọng trên điện cực tỷ lệ thuận với khối lượng tương đương của nguyên tố. Khối lượng tương đương của một chất là khối lượng mol của nó chia cho một số nguyên, tùy thuộc vào phản ứng hóa học mà chất đó có liên quan.
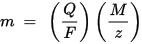
m là khối lượng của chất lắng đọng trên điện cực, Q là tổng điện tích truyền qua chất F = 96,485,33 (83) C mol - 1 là hằng số Faraday, M là khối lượng mol của chất (Ví dụ: khối lượng mol của nước H2O = 18 g / mol), z là số hóa trị của các ion của một chất (số electron trên mỗi ion).
Lưu ý rằng M / z là khối lượng tương đương của chất kết tủa. Đối với luật Faraday đầu tiên, M, F và z là hằng số, vì vậy giá trị của Q càng lớn, giá trị của m càng lớn. Đối với định luật Faraday thứ hai, Q, F và z là các hằng số, vì vậy giá trị của M / z (khối lượng tương đương) càng lớn, giá trị của m càng lớn.
Điện phân được sử dụng rộng rãi ngày nay trong công nghiệp và công nghệ. Ví dụ, đó là điện phân đóng vai trò là một trong những phương pháp hiệu quả nhất để sản xuất công nghiệp hydro, hydro peroxide, mangan dioxide, nhôm, natri, magiê, canxi và các chất khác. Điện phân được sử dụng để xử lý nước thải, trong mạ điện, mạ điện và cuối cùng là trong các nguồn hóa học. Nhưng điều đầu tiên trước tiên.
Thu được kim loại nguyên chất từ quặng bằng phương pháp điện phân
Nhờ điện phân, nhiều kim loại được chiết xuất từ quặng và được xử lý thêm. Vì vậy, khi quặng hoặc quặng đã làm giàu - cô đặc - được xử lý bằng thuốc thử, kim loại sẽ đi vào dung dịch, sau đó kim loại được tách ra khỏi dung dịch bằng phương pháp điện di. Kim loại nguyên chất được giải phóng cùng lúc tại cực âm. Bằng cách này nhận kẽm, đồng, cadmium.
Kim loại được xử lý điện hóa để loại bỏ tạp chất và chuyển đổi các tạp chất có trong dạng thuận tiện cho xử lý tiếp. Kim loại cần làm sạch được đúc dưới dạng các tấm, và các tấm này được sử dụng làm cực dương trong điện phân.
Khi dòng điện đi qua, kim loại của cực dương hòa tan, chuyển qua dạng cation vào dung dịch, sau đó các cation được thải ra ở cực âm và tạo thành kết tủa kim loại nguyên chất. Các tạp chất của cực dương không tan - chúng kết tủa với bùn anốt, hoặc đi vào chất điện phân, từ đó chúng được loại bỏ liên tục hoặc định kỳ.
Hãy xem xét như một ví dụ đồng điện tử. Thành phần chính của dung dịch - đồng sunfat - loại muối phổ biến nhất và rẻ nhất của kim loại này. Các giải pháp có độ dẫn điện thấp. Để tăng nó, axit sulfuric được thêm vào chất điện phân.
Ngoài ra, một lượng nhỏ chất phụ gia được đưa vào dung dịch để tạo điều kiện cho sự hình thành kết tủa kim loại nhỏ gọn. Nói chung, đồng, niken, chì, thiếc, bạc và vàng phải chịu quá trình tinh chế điện phân.
Xử lý nước thải điện phân
Điện phân được sử dụng trong xử lý nước thải (các quá trình đốt điện, điện cực và điện phân). Phương pháp làm sạch điện hóa là một trong những phương pháp được sử dụng phổ biến nhất. Đối với điện phân, các cực dương không hòa tan (từ tính, oxit chì, than chì, mangan, được lắng đọng trên một cơ sở titan), hoặc hòa tan (nhôm, sắt) được sử dụng.
Phương pháp này được sử dụng để phân lập các chất hữu cơ và vô cơ độc hại khỏi nước. Ví dụ, ống đồng được làm sạch quy mô bằng dung dịch axit sunfuric và nước thải công nghiệp sau đó phải được làm sạch bằng điện phân với cực dương không hòa tan. Đồng được giải phóng ở cực âm, một lần nữa có thể được sử dụng trong cùng một doanh nghiệp.
Nước thải kiềm được tinh chế bằng cách điện phân từ các hợp chất xyanua. Để tăng tốc quá trình oxy hóa xyanua, tăng độ dẫn điện và tiết kiệm năng lượng, một chất phụ gia ở dạng natri clorua được sử dụng trong nước.
Điện phân được thực hiện với cực dương than chì và cực âm thép. Cyanide bị phá hủy trong quá trình oxy hóa điện hóa và clo, được giải phóng trên cực dương. Hiệu quả của việc làm sạch như vậy là gần 100%.
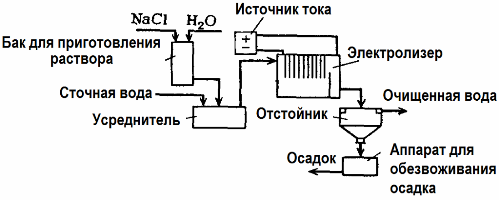
Ngoài việc làm sạch điện hóa trực tiếp, nó có thể được bao gồm trong quá trình điện phân đông máu. Không bao gồm việc bổ sung muối, điện phân được thực hiện với cực dương nhôm hoặc sắt hòa tan. Sau đó, không chỉ các chất gây ô nhiễm trên cực dương bị phá hủy, mà chính cực dương cũng tan biến. Các hợp chất phân tán hoạt động được hình thành mà các chất ô nhiễm phân tán keo tụ (làm dày).
Phương pháp này có hiệu quả trong việc xử lý nước thải từ chất béo, sản phẩm dầu, thuốc nhuộm, dầu, chất phóng xạ, v.v ... Nó được gọi là đốt điện.
Mạ điện
Mạ điện là sự lắng đọng điện phân của một số kim loại để bảo vệ sản phẩm khỏi bị ăn mòn và mang lại cho chúng vẻ ngoài thẩm mỹ thích hợp (lớp phủ được làm bằng crom, niken, bạc, vàng, bạch kim, v.v.). Vật này được làm sạch hoàn toàn, tẩy nhờn và được sử dụng làm cực âm trong bể điện phân trong đó dung dịch muối của kim loại cần phải phủ lên sản phẩm.
Một tấm kim loại giống nhau được sử dụng làm cực dương. Theo quy định, một cặp tấm anode được sử dụng và đối tượng được mạ kẽm được đặt giữa chúng.
Electroforming
Mạ điện - sự lắng đọng kim loại trên bề mặt của các cơ thể khác nhau để tái tạo hình dạng của chúng: khuôn để đúc các bộ phận, điêu khắc, in sáo, v.v.

Sự lắng đọng Galvanic của kim loại trên bề mặt của một vật thể chỉ có thể khi bề mặt này hoặc toàn bộ vật thể là một dây dẫn dòng điện, vì vậy nên sử dụng kim loại để tạo ra các mô hình hoặc hình thức. Kim loại dễ nóng chảy thích hợp nhất cho mục đích này: chì, thiếc, chất hàn, Hợp kim gỗ.
Những kim loại này mềm, dễ dàng xử lý với các công cụ kim loại, được khắc và đúc tốt. Sau khi xây dựng lớp mạ điện và hoàn thiện, kim loại khuôn được nung chảy từ thành phẩm.
Tuy nhiên, cơ hội lớn nhất cho các mô hình sản xuất vẫn được thể hiện bằng vật liệu điện môi. Để kim loại hóa các mô hình như vậy, cần phải cung cấp độ dẫn điện bề mặt của chúng. Thành công hay thất bại cuối cùng phụ thuộc chủ yếu vào chất lượng của lớp dẫn điện. Lớp này có thể được áp dụng theo một trong ba cách.
Cách phổ biến nhất là đồ họa hóa, nó phù hợp cho các mô hình plasticine và các vật liệu khác cho phép mài than chì trên bề mặt.
Bí quyết tiếp theo là bronzing, phương pháp này tốt cho các mô hình có hình dạng tương đối phức tạp, đối với các vật liệu khác nhau, tuy nhiên, do độ dày của lớp đồng, việc chuyển các bộ phận nhỏ có phần bị biến dạng.
Và cuối cùng mạ bạcphù hợp trong mọi trường hợp, nhưng đặc biệt không thể thiếu đối với những người mẫu dễ vỡ với hình dạng rất phức tạp - thực vật, côn trùng, v.v.
Nguồn hóa chất
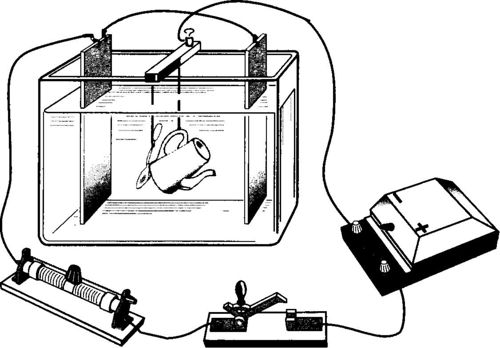
Ngoài ra, điện phân là quá trình chính do đó các nguồn hóa chất hiện đại nhất, chẳng hạn như pin và ắc quy, hoạt động. Có hai điện cực tiếp xúc với chất điện phân.
Một sự khác biệt tiềm năng được thiết lập giữa các điện cực - một lực điện động tương ứng với năng lượng tự do của phản ứng oxi hóa khử. Xem tại đây để biết thêm chi tiết: Nguồn hóa chất của dòng điện
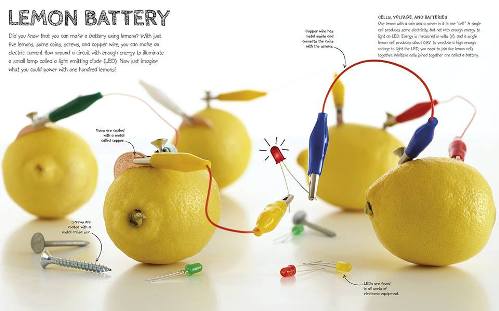
Lemon pin (bấm vào hình để phóng to)
Hoạt động của các nguồn dòng hóa học dựa trên sự xuất hiện của các quá trình phân tách không gian với mạch ngoài khép kín: trên cực dương âm, chất khử bị oxy hóa, các electron tự do được hình thành đi qua mạch ngoài tới cực âm dương, tạo ra dòng phóng điện, trong đó chúng tham gia vào phản ứng oxy hóa. Do đó, dòng điện tử mang điện tích âm dọc theo mạch ngoài đi từ cực dương đến cực âm, nghĩa là từ điện cực âm sang cực dương.
Xem thêm tại electro-vi.tomathouse.com
: